Nội dung từ Loigiaihay.Com
Đề bài
Người ta cho N2 và H2 vào trong bình kín dung tích không đổi và thực hiện phản ứng:
\({N_2}(g) + 3{H_2} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} 2N{H_3}\)
Sau một thời gian, nồng độ các chất trong bình như sau: [N2] = 2M; [H2] = 3M; [NH3] = 2M. Nồng độ mol/l của N2 và H2 ban đầu lần lượt là:
-
A.
3 và 6
-
B.
2 và 3
-
C.
4 và 8
-
D.
2 và 4
Phương pháp giải
Dựa vào kiến thức về cân bằng hóa học
Lời giải của GV HocTot.XYZ
Gọi nồng độ ban đầu của N2 và H2 là a và b
Ta có: [N2] = [H2]/3 = [NH3]/2
\(a - 2 = \frac{{b - 3}}{3} = \frac{2}{2}\)
a = 3 và b = 6
Đáp án A đúng
Đáp án : A
Mở rộng
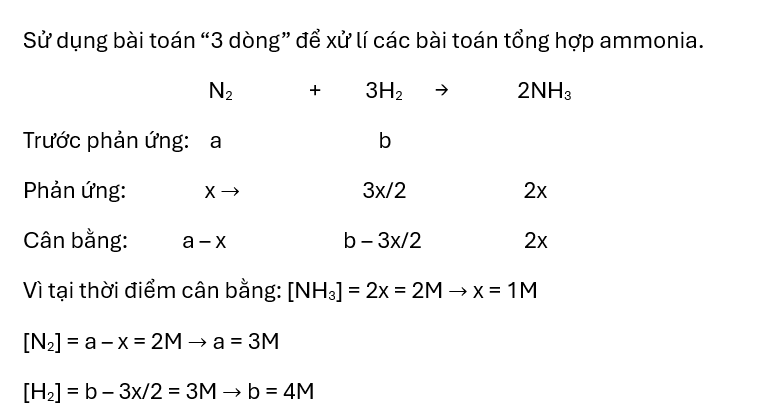
Có thể áp dụng cho các bài toán khác, chỉ cần thay lại số liệu phù hợp với bài toán.

Các bài tập cùng chuyên đề













Danh sách bình luận