Nội dung từ Loigiaihay.Com
Khi dùng chlorine để khử trùng hồ bơi, chlorine sẽ phản ứng với urea trong nước tiểu và mồ hôi người tắm, tạo hợp chất nitrogen trichloride (NCl3), gây ra nhiều tác động xấu đến sức khỏe như đỏ mắt, hen suyễn,…
Viết công thức Lewis của nitrogen trichloride
Bước 1: Tổng số electron hóa trị của phân tử
Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử
Bước 3: Tính số electron hóa trị chưa tham gia liên kết trong sơ đồ. Hoàn thiện octet cho các nguyên tử
Bước 4: Chuyển cặp electron chưa liên kết trên nguyên tử xung quanh thành electron liên kết sao cho nguyên tử trung tâm thỏa mãn quy tắc octet
Bước 1: Tổng electron hóa trị của phân tử NCl3: 5.1 + 7.3 = 26
Bước 2: Khung sơ đồ biểu diễn liên kết của phân tử NCl3
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là:
26 – 2.3 = 20
Hoàn thiện octet cho các nguyên tử có độ âm điện lớn hơn trong sơ đồ (Cl có độ âm điện lớn hơn)
- Số electron hóa trị còn lại: 20 – 6.3 = 2
Nguyên tử trung tâm N chưa đạt octet, dùng 2 electron còn lại tạo octet cho N.
Công thức Lewis của nitrogen trichloride (NCl3) là:

Các bài tập cùng chuyên đề
Bài 1 :
Để hình thành phân tử phosphorus trichloride (PCl3) thì mỗi nguyên tử chlorine và phosphorus đã góp chung bao nhiêu electron hóa trị? Viết công thức Lewis của phân tử
Bài 2 :
Theo độ âm điện, boron trifluoride là hợp chất ion, thực tế nó là hợp chất cộng hóa trị, với công thức Lewis như sau:
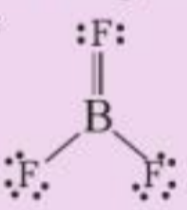
a) Viết phương trình hóa học tạo chất trên từ các đơn chất
b) Phân tử BF3 có bao nhiêu liên kết σ và bao nhiêu liên kết п?
Bài 3 :
Viết công thức electron, công thức Lewis và công thức cấu tạo của Cl2, H2O, CH4
Bài 4 :
Viết công thức Lewis của các phân tử CS2, SCl2 và CCl4
Bài 5 :
Viết công thức Lewis của PCl5 và SF6
Bài 6 :
Viết công thức Lewis và xác định dạng hình học của CS2. Xác định dạng lai hóa của nguyên tử trung tâm C trong phân tử này.
Bài 7 :
Xác định công thức Lewis của nitric acid HNO3. Cho biết nguyên tử H liên kết với O mà không phải với N.
Bài 8 :
Viết công thức Lewis của CF4, C2H6, C2H4 và C2H2
Bài 9 :
Các điện tích cùng dấu thì đẩy nhau hay hút nhau?
Bài 10 :
Viết công thức Lewis của CH4, BF3, SO3, F2O
Bài 11 :
Viết công thức cấu tạo của CO2 và H2O
Bài 12 :
Những electron như thế nào được gọi là:
a) Electron hóa trị
b) Electron chung
c) Electron hóa trị riêng
Bài 13 :
Mở đầu: Theo em, dạng hình học nào sau đây của hai phân tử carbon dioxide và nước là đúng?
Bài 14 :
Trình bày sự tạo thành liên kết hóa học trong các phân tử sau dựa vào sự lai hóa của các nguyên tử trung tâm:
a) C2H2
b) C2H4
c) NH3
Bài 15 :
Viết công thức VSEPR và dự đoán hình học của các phân tử sau:
a) HCN
b) SO3
c) PH3
Bài 16 :
Viết công thức Lewis của các phân tử sau:
a) HCN
b) SO3
Bài 17 :
Viết công thức VSEPR của H2O, NH3 và SO2
Bài 18 :
Theo công thức Lewis của nước, phân tử nước có bao nhiêu cặp electron chung và bao nhiêu cặp electron riêng ở nguyên tử trung tâm?
Bài 19 :
Viết công thức Lewis của phân tử CCl4
Bài 20 :
Hãy tính tổng số electron hóa trị của phân tử BF3
Bài 21 :
Viết công thức electron của phân tử methane (CH4)
Bài 22 :
Viết công thức Lewis của nguyên tử oxygen và nguyên tử magnesium.
Bài 23 :
Cho các phân tử NCl3, SO3, CO2
a) Nguyên tử trung tâm trong các phân tử trên ở trạng thái lai hóa nào?
b) Phân tử nào không phân cực, phân tử nào phân cực? Vì sao?
Bài 24 :
Viết công thức của một số phân tử sau theo mô hình VSEPR: CCl4, H2S, CO2, SO3 và PH3. Nêu số cặp electron hóa trị liên kết và chưa liên kết trong mỗi phân tử
Bài 25 :
Công thức Lewis của NO2 là

Bài 26 :
Viết các công thức Lewis cho mỗi phân tử sau:
a) Cl2, N2
b) SO2, SO3
c) H2O, H2S, HOCl
Bài 27 :
Trình bày các bước để viết công thức Lewis của phân tử NH3
Công thức cấu tạo của CO2 là O = C = O
Công thức cấu tạo của H2O là H – O – H
Bài 28 :
Công thức Lewis của CS2 là
Bài 29 :
Dạng hình học phân tử ảnh hưởng đến khả năng phản ứng, hoạt tính sinh học, tính phân cực,… của phân tử. Dựa trên cơ sở nào để dự đoán dạng hình học của một phân tử
Bài 30 :
Thiết lập công thức Lewis cho các phân tử H2O, NH3 và CH4. Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?













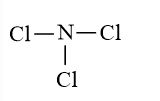
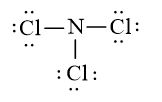
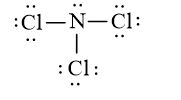


Danh sách bình luận