Viết các công thức Lewis cho mỗi phân tử sau:
a) Cl2, N2
b) SO2, SO3
c) H2O, H2S, HOCl
Bước 1: Xác định tổng electron hóa trị trong phân tử
Bước 2: Vẽ khung phân tử
Bước 3: Điền các electron hóa trị chưa tham gia liên kết vào các nguyên tử xung quanh
Bước 4: Tính số electron hóa trị còn lại
a) Cl2
Bước 1: Cl có 7 electron hóa trị
=> Tổng electron hóa trị Cl2 = 7.2 = 14 electron
Bước 2: Vẽ khung phân tử với các liên kết đơn
Cl - Cl
Bước 3: Mỗi nguyên tử Cl cần 6 electron hóa trị để đạt octet
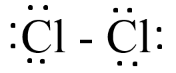
Bước 4:
- Số electron hóa trị còn lại = 14 – 2.6 – 1.2 = 0
=> Công thức Lewis của Cl2
N2
Bước 1: N có 5 electron hóa trị
=> Tổng electron hóa trị N2 = 5.2 = 10 electron
Bước 2: Vẽ khung phân tử với các liên kết đơn
N - N
Bước 3: Hoàn thiện octet cho nguyên tử N
Bước 4:
- Số electron hóa trị còn lại là: 10 – 6.2 – 2.1 = - 4
- Số electron hóa trị của nguyên tử N là 5, nên để đạt octet mỗi nguyên tử N sẽ góp chung 3 electron hóa trị để tạo liên kết với nhau.
Công thức Lewis của phân tử N2 là
b) SO2
Bước 1: S có 6 electron hóa trị, O có 6 electron hóa trị
=> Tổng electron hóa trị SO2 = 6 + 6.2 = 18 electron
Bước 2: Vẽ khung phân tử với các liên kết đơn
O – S - O
Bước 3: Hoàn thiện octet cho nguyên tử O
Bước 4:
- Số electron hóa trị còn lại là: 18 – 6.2 – 2.2 = 2
- Nguyên tử S có 4 electron hóa trị nên 1 nguyên tử O sẽ dùng 1 cặp electron để tạo liên kết với S và nguyên tử S còn 1 đôi electron chưa tham gia liên kết.
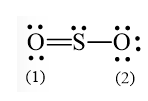
SO3
Bước 1: S có 6 electron hóa trị, O có 6 electron hóa trị. Trong phân tử SO3, có 1 nguyên tử S và 3 nguyên tử O
⇒ Tổng số electron hóa trị = 1.6 + 3.6 = 24 electron
Bước 3: Mỗi nguyên tử O cần 6 electron để đạt octet.
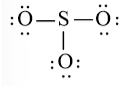
Bước 4: Số electron hóa trị còn lại là: 24 – 2.3 – 6.3 = 0
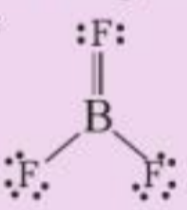
Tuy nhiên S chưa đủ octet nên ta chuyển 1 cặp electron của nguyên tử O tạo thành cặp electron dùng chung.
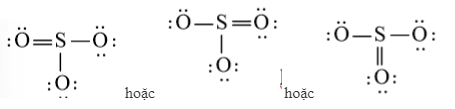
c) H2O
Bước 1. Tổng số electron hóa trị là 1.2 + 1.6 = 8
Bước 2. Trong phân tử H2O, nguyên tử O cần 2 electron để đạt octet, nguyên tử H cần 1 electron hóa trị để đạt octet. Vì vậy, O là nguyên tử trung tâm, còn các nguyên tử H được xếp xung quanh.
H – O – H.
Bước 3. Nguyên tử H đã đạt octet.
Bước 4. Số electron hóa trị còn lại là: 8 – 2.2 = 4
Nguyên tử O có 4 electron hóa trị nên sẽ chuyển 4 electron còn lại cho O để nguyên tử O đạt octet.
Công thức Lewis của H2O là:
H2S
Bước 1. Tổng số electron hóa trị của phân tử = 1.2 + 1.6 = 8 electron
Bước 2. Trong phân tử H2S, nguyên tử S cần 2 electron để đạt octet, nguyên tử H cần 1 electron để đạt octet. Vì vậy, nguyên tử S là nguyên tử trung tâm, còn 2 nguyên tử H được xếp xung quanh:
H – S – H
Bước 3. 2 nguyên tử H đã đạt octet.
Bước 4. Số electron hóa trị còn lại = 8 – 2.2 = 4
Nguyên tử S có 4 electron hóa trị nên để đạt octet thì chuyển 4 electron còn lại cho nguyên tử S.
Công thức Lewis của H2S là:
HOCl
Bước 1. Tổng số electron hóa trị của phân tử = 1.1 + 1.6 + 1.7 = 14 electron.
Bước 2. Trong phân tử HOCl, nguyên tử Cl cần 1 electron để đạt octet, nguyên tử O cần 2 electron để đạt octet, nguyên tử H cần 1 electron để đạt octet. Vì vậy, O là nguyên tử trung tâm, nguyên tử H và Cl được xếp xung quanh:
H – O – Cl
Bước 3. Nguyên tử H đã đạt octet, nguyên tử Cl cần 6 electron hóa trị để đạt octet:
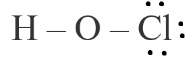
Bước 4. Số electron hóa trị còn lại = 14 – 2.2 – 3.2 = 4
Nguyên tử O có 4 electron hóa trị nên sẽ chuyển 4 electron còn lại cho O để nguyên tử O đạt octet.
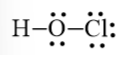














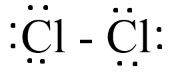
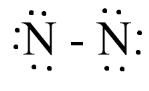
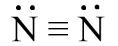
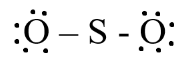
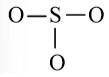
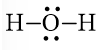
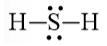



Danh sách bình luận